Innhold: Kirurgi
Kirurgi
Kirurgi vid UC
Akut kirurgi
Indikationer för brådskande/akut operation är toxisk dilata- tion med allmänpåverkan vid fulminant kolit, intraktabel blödning eller perforation och akut svår kolit som inte svarar på intensifierad medicinsk behandling inom 5–7 dagar.
Vanligen görs då en subtotal kolektomi, ileostomi och bevarande samt förslutning av rektum, alternativt anlägg- ande av en s. k. mukotan fistel.
I lugnt skede kan senare eventuell restorativ kirurgi genomföras med antingen IRA (förutsatt att rektum för-bättrats och är läkt eller endast milt inflammerad) eller med sk bäckenreservoir (pouch) av tunntarm (vanligen av J-typ) och ileal pouch-anal anastomos (IPAA).
Elektiv kirurgi
Indikationer:
- Kronisk kontinuerlig sjukdom.
- Cancerprofylax, fynd av dysplasi eller cancer.
- Tillväxthämning.
- Patientens önskan.
- Restorativ kirurgi efter akut kolektomi.
1. Bäckenreservoir
Kolektomi görs i höjd strax ovanför linea dentata med bibe- hållande av sfinkterapparaten och konstruktion av bäcken- reservoir och IPAA är en av de vanligaste elektiva opera- tionstyperna. Bäckenreservoir görs numera vanligen med s. k. stapling teknik, vilket vanligen innebär att någon eller maximalt några centimeter av rektalslemhinnan blir kvar.
Fördelen mot den tidigare s.k. mukosektomin är framför allt kortare operationstid och mindre risk för läckage till följd av minskad påfrestning på sfinkterapparaten under operationen. Inflammation i kvarvarande restbräm av rek- talslemhinna kan dock förekomma liksom även en (mycket liten) kvarvarande risk för neoplasi, se Bild 14. Patienten har ofta 5–7 tarmtömningar per dygn, ev. med 1–2 nattetid.

Bild 14.
Bäckenreservoir av s.k. J-typ. Tillförande del av tunntarmen resp. blind del.
2. IRA
I de fall där rektum är läkt eller endast uppvisar en lätt inflammation kan IRA övervägas. De funktionella resul-taten är i klass med de vid bäckenreservoir (3–6 tarmtöm-ningar/dag i genomsnitt). IRA innebär dock att en viss risk för nya skov kvarstår samt även en viss risk för neoplasi-utveckling hos dem med tidigare extensiv kolit. IRA är mindre lämpligt vid kolektomi p. g. a. höggradig dysplasi eller cancer, PSC eller vid svårbehandlad proktit.
2. IRA
I de fall där rektum är läkt eller endast uppvisar en lätt inflammation kan IRA övervägas. De funktionella resul-taten är i klass med de vid bäckenreservoir (3–6 tarmtöm-ningar/dag i genomsnitt). IRA innebär dock att en viss risk för nya skov kvarstår samt även en viss risk för neoplasi-utveckling hos dem med tidigare extensiv kolit. IRA är mindre lämpligt vid kolektomi p. g. a. höggradig dysplasi eller cancer, PSC eller vid svårbehandlad proktit.
3. Stomi
Proktokolektomi med konventionell ileostomi är dock fort-farande ett alternativ, framför allt hos äldre patienter.
4. Kockreservoir
Kontinent ileostomi s. k. ”Kockreservoir” vid UC är numera ett ovanligt ingrepp och innebär en reservoir innanför främre bukväggen med en ”nippel” av tunntarm som sluter tätt mot den yttre, slitsformade ca 5–7 mm stora hudöpp-ningen (Bild 15).
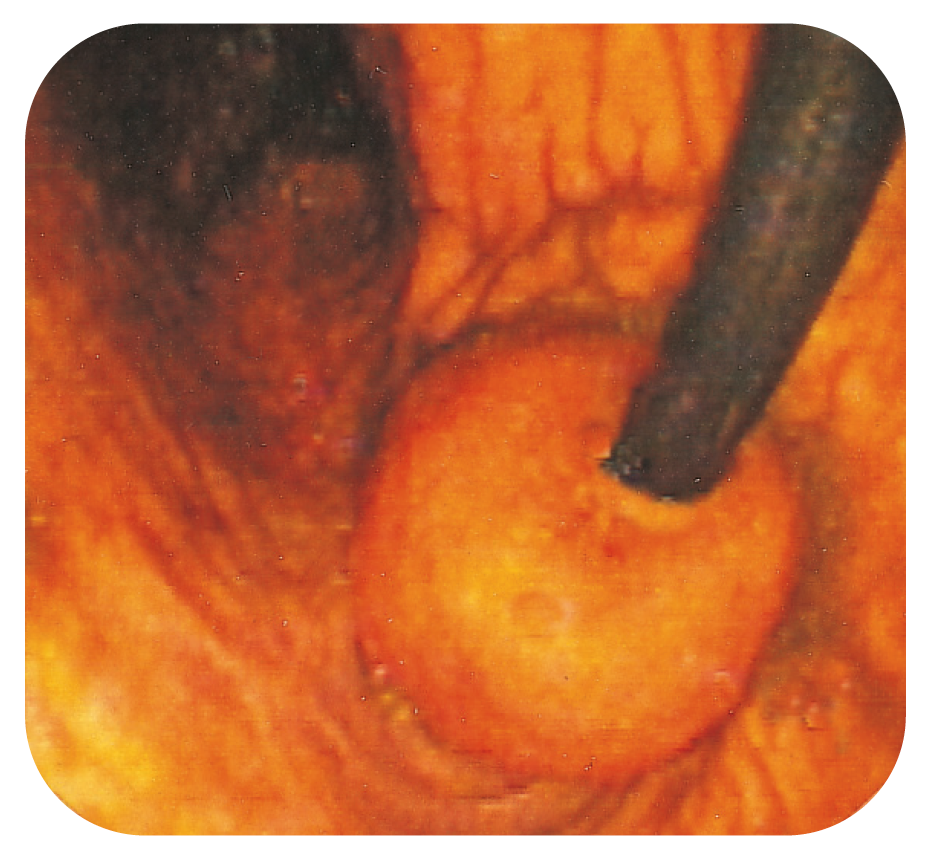
Bild 15.
Den inre nippeln i en kontinent ileostomi ad modum Kock.
Pouchit
Episoder med vattniga diarréer, inkontinens, smärta, blöd- ning och ibland feber och illamående i kombination med endoskopiska tecken på inflammation i reservoirslemhin-nan har gett upphov till ett nytt IBD-liknande tillstånd som benämns ”pouchit”. Endoskopi visar akut inflam-mation med svullen, rodnad, lättblödande och pusbelagd slemhinna. Histopatologin visar ospecifik inflammatorisk bild och ibland även villös atrofi. Diagnosen blir oftast symptombaserad. Den kumulativa risken är ca 40–50 % inom 5 år efter operationen. Pouchit behandlas i de flesta fall effektivt med metronidazol (Flagyl®) under 2–4 veckor. Ett alternativ till oral behandling kan vara metronidazol-vagitorier som lokalbehandling. Ciprofloxacin är ett ofta använt alternativ. Ett licensläkemedel, alicaforsen, som är en antisen-soligonukleotid som hämmar ICAM-1 kan vara effektivt vid pouchit men ytterligare studier behövs för att få tillräcklig evidens. För underhållsbehandling av pouchit rekommenderar ECCO guidelines VSL#3®.
En liten subgrupp av patienter utvecklar atrofi i reservoir-mucosan, men risken att dysplastiska förändringar ska upp-stå har visat sig vara mycket liten efter 35 års uppföljning av patienter opererade i Sverige och USA.
Kirurgi vid CD
Behandlingen av CD uppfattades bland annat av professor Burrill Crohn själv som primärt kirurgisk med resektion av det afficierade tarmavsnittet. Ganska snart stod det emeller-tid klart att sjukdomen hade en mycket hög recidivfrekvens efter kirurgisk terapi.
Principen med väl tilltagna resektioner med god mar-ginal mellan makroskopiskt sjuk och frisk tarm visade sig inte minska recidivrisken, snarare tvärtom. Vid begränsad ileocekalresektion av klassisk ileocekal CD är den sympto-matiska recidivrisken efter ett år ca 20 %, efter fem år 50 % och efter tio år 70 %. Recidiv kommer oftast mycket tidigt, redan efter några månader postoperativt och ses makrosko-piskt först i form av aftösa ulcerationer i neoterminala ileum precis proximalt om anastomosen till kolon. Risken för en ny operation är ca 40 % efter tio år. En begränsad ileocekal resektion är ändå ett alternativ till medicinsk behandling vid denna sjukdomslokalisation eftersom fler än hälften av patienterna kan klara sig utmärkt under lång tid utan tillägg av medicinsk terapi.
Kirurgisk behandling vid CD är i första hand riktad mot komplikationer som abscesser, enterokutana eller enteroen-terala fistlar, samt fibrösa stenoser. Strategin är att genom-föra minsta möjliga ingrepp, numera ofta laparoskopiskt, och med användande av tarmbevarande kirurgi så långt det är möjligt. Ny teknik innebär strikturplastik (”öppna på längden – sy ihop på tvären”) och/eller korta, eventu-ella multipla, resektioner. Vid tillväxthämning hos barn måste resektion övervägas tidigt i förloppet. För att mini-mera resektionens omfattning rekommenderas peroperativ enteroskopi (eventuellt via liten enterostomi) för optimal evaluering av förändringarna på mukosasidan.
Akut svårt skov av CD i kolon (och rektum) eller behand-lingsrefraktär kronisk kontinuerlig Crohn-kolit är en annan indikation för kirurgi, vanligen innebärande kolektomi med förslutning av rektum samt ileostomi. Totalt sett blir dock en permanent ileostomi nödvändig i färre än 10 % av CD-fallen där den övervägande majoriteten har kolonen-gagemang. Vid fistulerande perianal-anorektal sjukdom är dock långtidsprognosen för rektum dålig och rektumexstir-pation blir förr eller senare oftast aktuellt.
Restorativ operation med bäckenreservoir är generellt sett kontraindicerad vid CD, särskilt i de fall där fistu-lerande anorektalt engagemang förekommit. I vissa fall, med obestämbar kolit eller ulcerosaliknande Crohn-kolit utan tunntarmsengagemang (t. ex. då endast mikroskopiska fynd av granulom talar för CD) kan ibland bäckenreservoir ändå övervägas. Sjukdomen bör då ha varit i remission en längre tid (helst >5 år). Aktuella studier talar för att långtidsresultaten i vissa fall är i paritet med de som ses vid restorativ operation p. g. a. UC. Ileorektal anastomos (IRA) är ett annat alternativ som kan övervägas om rektum inte är allvarligt inflammerad. Recidivrisken är dock ca 50 %. Både vid reservoir och IRA finns möjligheten att senare konvertera till en ileostomi. Den ”extra” tid, kanske flera år, med kontinent tarmfunktion kan vara nog så viktigt för en ung person som t. ex. håller på att bilda familj. En upp-skjuten ”slutoperation” kan då vara ett rimligt övervägande i det totala omhändertagandet av patienten. Operation med kontinent ileostomi (s. k. Kocksreservoir) anses vara relativt kontraindicerad vid CD, men kan övervägas om patienten inte uppvisat några tecken på CD i tunntarmen. Patienten med CD har en något ökad operationsmorbiditet (framför allt septiska komplikationer, sårinfektioner, fistlar) och på lång sikt är risken för ileus 10–20 %.
Postoperativ recidivförebyggande medicinsk behandling
Flera stora studier har undersökt värdet av postoperativt given långtidsbehandling med 5-ASA men entydiga resultat från kontrollerade studier som stöder en allmän strategi med detta förfaringssätt föreligger inte ännu. Det kan vara befogat att överväga recidivförebyggande behandling i vissa högriskgrupper, t. ex. patienter med täta upprepade post-operativa recidiv eller vid annan komplikation såsom kronisk blödning. Långtidsbehandling med azatioprin/6-MP är effektivt som profylax efter resektion, liksom direkt postoperativ behandling med per oral metronidazol i tre mån-ader. För de svårast sjuka patienterna (flera resektioner, täta recidiv) blir biologisk underhållsbehandling ofta nödvändig.
Komplikationer til CD
Perianal CD
Perianala abscesser och fistlar är vanliga komplikationer till CD och ses hos 30–50 % av patienterna. CD bör uteslutas vid komplicerade och/eller återkommande perianala fistlar hos icke-IBD-patient eftersom upp till 45 % av CD debu-terar som perianal sjukdom. Perianal CD kräver många gånger multidisciplinär bedömning med gastroenterolog, kolorektalkirurg och radiolog, Behandling består av seton, antibiotika, immunomodulering och anti-TNF-behandling med målsättningen att minimera symptomen och bevara kontinensen.
Perianal abscess
Ofta akut debut med smärta, ömmande perianal resistens och ev. feber. Ska remitteras akut till kirurg för dränering. Antibiotika ges vid feber/allmänpåverkan (ciprofloxacin och/eller metronidazol). Det krävs en erfaren kolorek-talkirurg för åtgärd av eventuell fistel med t. ex. seton i det akuta skedet. Det är lätt att förvärra fistelsjukdomen och man bör om möjligt först ge abscessen en chans att spontanläka innan vidare åtgärd av bakomliggande fistel. Dränering är väsentligt innan immunsupprimerande behandling initieras. Redan pågående tiopurinbehand-ling kan fortgå men pågående biologisk behandling pau-sas tills abscessen är dränerad.
Perianal fistel
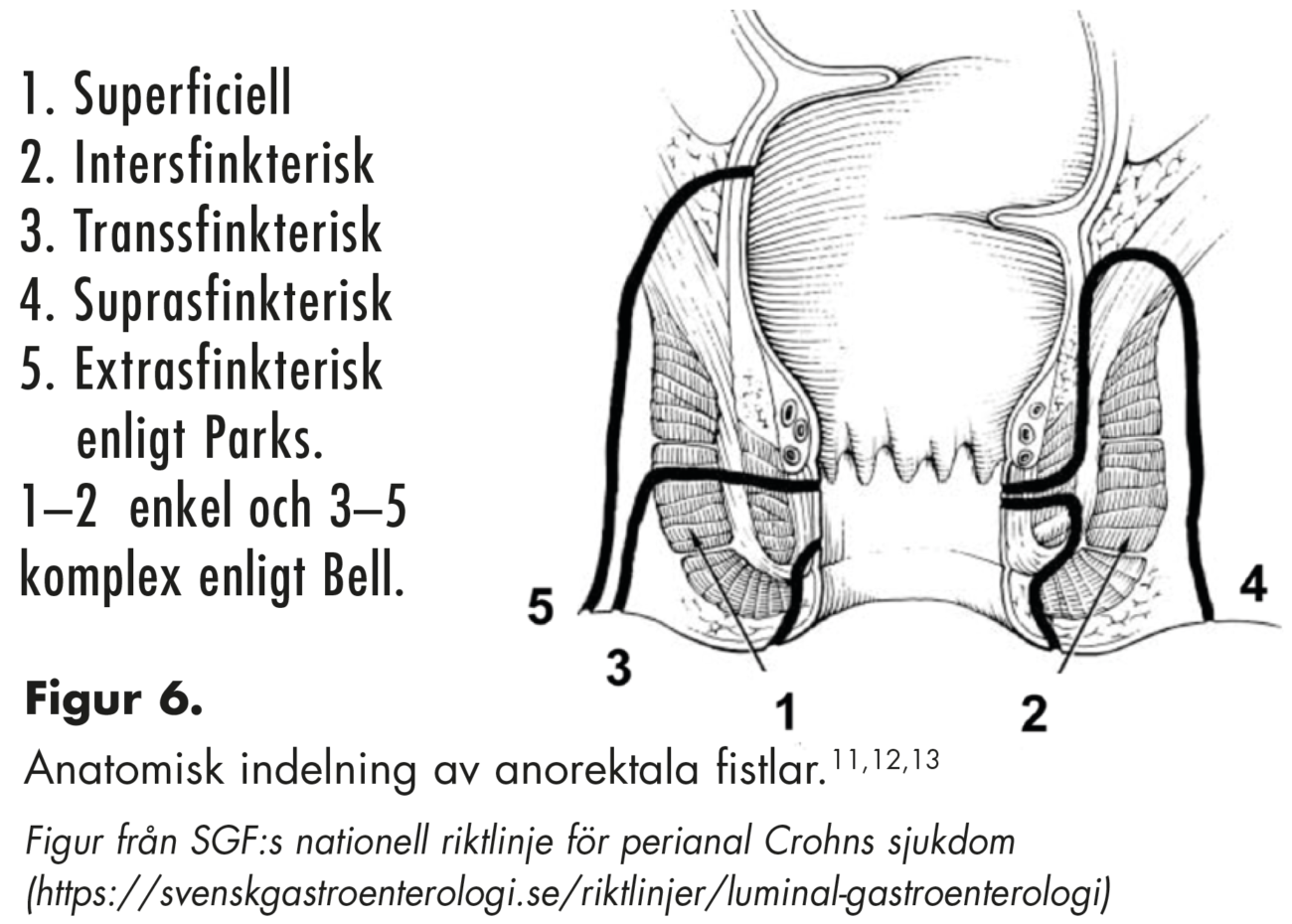
Perianala fistlar ses hos ca 10–15 % av patienterna, varav drygt en tredjedel hos de med kolorektal utbredning. En klassisk kombination är även ileocekal CD med perianal fistelsjukdom. Fistlar är oftast solitära men en komplex bild med multipla och komplicerade runt analkanalen (s.k. hästskofistlar) och till rektum förekommer. Fistlar beskrivs enligt den anatomiska utbredningen i förhållande till sfink-tern enligt Parks samt enkel eller komplex enligt Bell.
Vanliga symptom är sekretion och ömhet/smärta. Fistelaktiviteten är vanligen kopplad till underliggande rek-tal inflammation och det är inte möjligt att läka fistelsjuk-domen om inte slemhinneläkning uppnås först. Diagnostik och kartläggning sker med åtminstone två av de tre metoder-na MR, 3D analt ultraljud och/eller undersökning i narkos. Asymptomatiska fistlar bör ej behandlas. Symptomatiska fistlar behandlas i första hand med ciprofloxacin 500 mg x 2 och/eller metronidazol 400 mg x 3 under begränsad tid. Lös seton anlägges därefter av kirurg. Tiopuriner är lämp-lig förstahandsbehandling men vid komplicerad/aggressiv sjukdom kan anti-TNF vara indicerat tidigt i förloppet. IFX är det enda biologiska läkemedlet med indikationen fistulerande CD. Det är viktigt att fisteln är dränerad i 2–4 veckor med seton innan biologisk behandling insättes för att undvika abscessbildning/sepsis. Anti-TNF kan få fistlar att sluta sig, men för varaktig läkning krävs ofta även upprepad kirurgisk intervention. Seton bör åtminstone sitta kvar fram till planerad kirurgi. De vanligaste kirurgiska åtgärderna är klyvning (ytliga fistlar), kollagenplugg och ”advancement flap”, där den inre mynningen försluts. Setonen kan dras efter andra induktionsdosen om kirurgi ej planeras alterna-tivt sitta kvar som långtidslösning.
Övriga komplikationer till CD
- INTRAABDOMINELLA FISTLAR
Dessa uppstår oftast proximalt om ett stenoserat tarm-segment eller ovan en sfinkter (ileocekalvalveln, anus). Rektovaginala och rektovesikala fistlar är ovanliga och svårbehandlade. Det sistnämnda kan ge pneumaturi. Vid penetrerande inflammation kan perforation till fri bukhåla uppkomma alternativt med fistulering till annan tarmslynga (enteroenterala fistlar) eller till bukvägg (entero-kutana fistlar), men dessa är dock sällsynta komplikationer. Vid svår ileocekal CD kan en inflammatorisk ”kaka” med komplext fistelsystem samt (mikro)abscesser förekomma. Detta tillstånd är svårt att behandla i det akuta skedet med kirurgisk resektion. Steroider eller biologisk behandling är inte heller lämpligt initialt pga risken för sepsis. Avlastande loopileostomi proximalt om inflammationen kan vara en intial temporär lösning för att området ska ”kyla av” inför kirurgisk åtgärd och medicinsk behandling.
- KOLERETISK DIARRÉ
Till följd av försämrad återabsorption av gallsyror i dis-tala ileum vid aktiv inflammation eller (vanligare) efter resektion. En ökad mängd gallsyror når då kolon och verkar direkt retande på kolonslemhinnan med vattnig diarré som följd. Tillståndet uppkommer framför allt efter resektion av mer än 50 cm ileum, men ibland även efter kortare resektioner.
- MALABSORPTION
Kliniskt betydelsefull fettmalabsorption ses oftast först om mer än en meter tunntarm resecerats. Vid upprepade och längre resektioner kan man se malabsorption av vissa spår- metaller (t.ex. Mg++), elektrolyter, fettlösliga vita-miner (A, D, E, K) samt järn och folat. Absorptionen av vitamin B12 sker i distala ileum och redan mindre inflammation och/ eller resektion kan leda till B12-brist. Inte sällan föreligger även folsyrebrist. Om bara ca en meter återstår finns risk för s. k. ”korttarm”-syndrom, som dock nu för tiden blivit mycket ovanligt till följd av konservativ kirurgisk strategi och ökad långtidsterapi med immunmodulerande behandling. Vid tunntarms-CD i kombination med ileostomi är risken stor även för generell malabsorption och vätskeförluster. Se vidare under ”Nutrition vid IBD” (sidan 92).
- KONKREMENT
CD-patienter, särskilt de som genomgått tunntarmsresek- tion, anses ha en ökad risk för gallsten liksom även för njursten (oxalatstenar p. g. a. hyperoxaluri).
- BAKTERIELL ÖVERVÄXT
Stenoser till följd av fibrotiska strikturer eller inflammato-riskt trånga partier kan, liksom även borttagande av ileoce-kalvalveln, ge upphov till patologiskt ökad bakterieflora i tunntarmen. Ökade diarrébesvär kan bli följden.
- ILEUS
Kan uppstå till följd av inflammation och senare fibros med strikturering/stenosering av lumen, framför allt i dis-tala ileum. Vanligast är dock relativ stenosering med kortare och oftast spontant övergående smärtattacker (oegentligt kallat subileus) efter intag av svårdigererad föda som t.ex. svamp, trådig frukt, nötter eller liknande. I de flesta fall av relativ stenosering är expektans med avlastning och i. v. dropp tillräckligt, ibland med tillförsel av röntgenkontrast (Gastrografin®). Patienter som tidigare opererats löper dess-utom en ökad risk för bridileus till följd av adherensbildning.
- ANEMI
Vid CD beror anemi ofta på en kombination av benmärgs- hämning till följd av inflammation, järnbrist på grund av blodförluster från tarmen samt B12-malabsorption på grund av inflammation i terminala ileum eller på grund av resektion av denna del av tunntarmen. Även en generell malabsorption (inkl järn, folsyra) kan ge anemi.
Järnsubsitution ges med fördel intravenöst. Moderna preparat som kan ges i högdos i.v., t. ex. Ferinject® och Monofer®, ger tämligen snabb effekt symptomatiskt och efter 6–8 veckor är Hb-värdena ofta återställda.
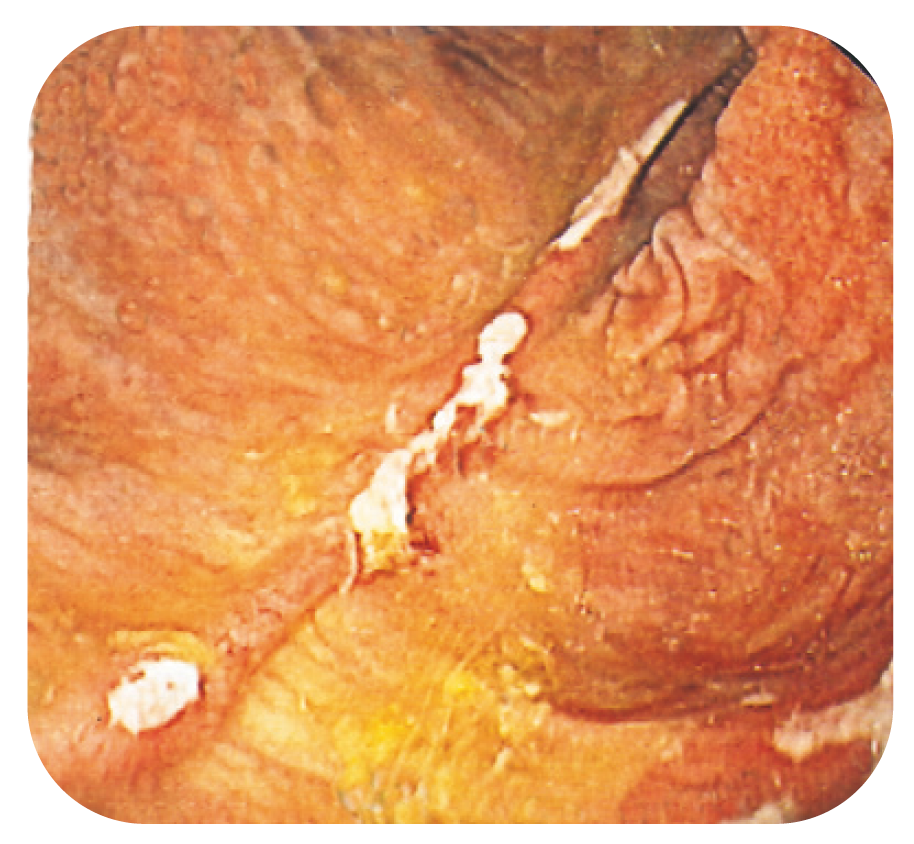
Bild 16.
Tydliga anastomoslinjer med ställvist före-kommande fibrinbeslag i bäckenreservoir hos patient med CD som ursprunglig diagnos.
